日野智也 研究内容
膜タンパク質の構造生命科学と産業応用を目指した研究
細胞は脂質からできた生体膜を用いて自己と外部環境とを区分けしています。脂質は水溶性物質を透過しにくい性質を持つため、生命活動を維持するためには、生体膜を介した物質のやり取りや、外部環境の情報感知及び細胞内への情報伝達等を正確に行う特別な仕組みが必要です。膜タンパク質は、水溶液に溶け込むことができる通常のタンパク質とは異なり、生体膜に付着あるいは貫通する性質を持ち、上述のような生命にとって必須な機能を担うタンパク質の一群です。
日野准教授のグループでは、これら膜タンパク質に焦点を絞り、その立体構造決定により膜タンパク質の機能を解明する膜タンパク質構造生命科学を展開し、さらに立体構造情報を活用した創薬や産業応用を目指した研究を行っています。
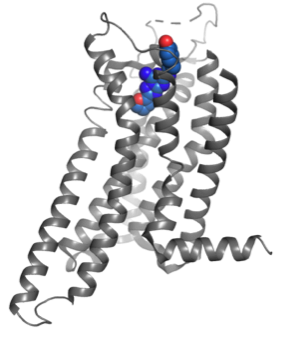
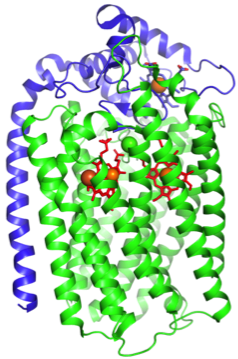
現在、多様な膜タンパク質の立体構造決定に取り組むとともに、立体構造情報を活用した創薬や産業応用を目指した研究を行っています。
以下では最近取り組んでいる具体的な研究テーマを紹介します。
1. 生物における温度感知の分子機構解明
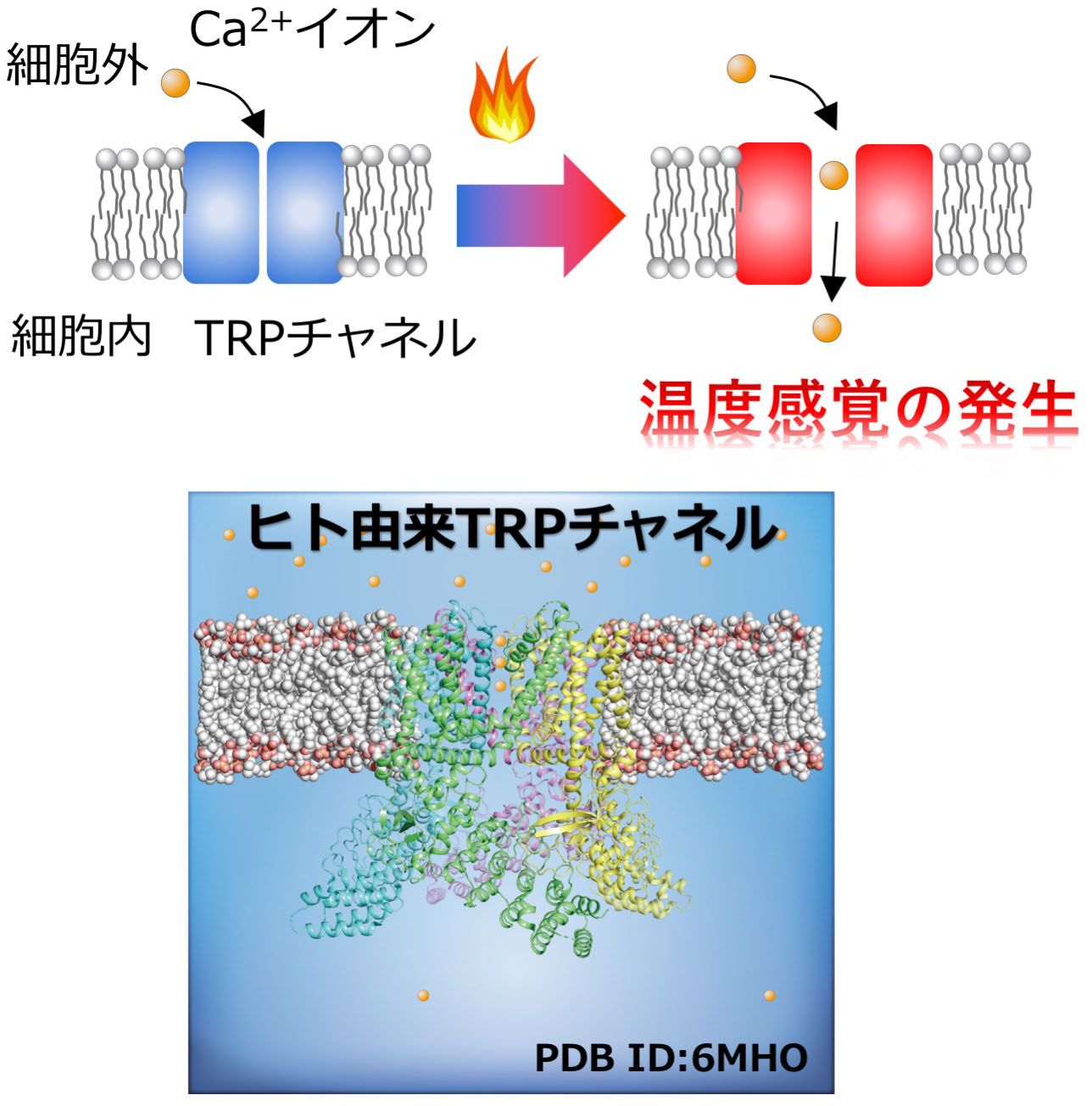 私たちは季節の移り変わりによる外気温の変化を感じとることができます。この我々に身近な生理機能には、温度変化に応じて活性化する膜タンパク質TRPイオンチャネルが関わっています。ヒトにおいては、異なる温度域に応じて活性化するTRPイオンチャネルが複数存在するため、17℃以下の低温を冷たい、25℃近辺を温かい、43℃以上を熱いと感じることができます。私たちは、これらのTRPイオンチャネルが温度を感知する仕組みを原子レベルで理解することを目的に、結晶構造解析やクライオ電子顕微鏡など最新の解析技術を用いた立体構造解析に取り組んでいます。
私たちは季節の移り変わりによる外気温の変化を感じとることができます。この我々に身近な生理機能には、温度変化に応じて活性化する膜タンパク質TRPイオンチャネルが関わっています。ヒトにおいては、異なる温度域に応じて活性化するTRPイオンチャネルが複数存在するため、17℃以下の低温を冷たい、25℃近辺を温かい、43℃以上を熱いと感じることができます。私たちは、これらのTRPイオンチャネルが温度を感知する仕組みを原子レベルで理解することを目的に、結晶構造解析やクライオ電子顕微鏡など最新の解析技術を用いた立体構造解析に取り組んでいます。
2. 薬の標的となる膜タンパク質の立体構造解明と創薬
 多くの医薬品は、細胞表面に露出した膜タンパク質分子を標的とし、これらの活性を調節することで細胞内の状態を制御して薬効を発揮します。したがって、薬剤の標的となる膜タンパク質の立体構造を決定し、その機能を詳細に理解することができれば、これらの膜タンパク質の機能を制御できる新たな薬剤分子をデザイン可能になります。
多くの医薬品は、細胞表面に露出した膜タンパク質分子を標的とし、これらの活性を調節することで細胞内の状態を制御して薬効を発揮します。したがって、薬剤の標的となる膜タンパク質の立体構造を決定し、その機能を詳細に理解することができれば、これらの膜タンパク質の機能を制御できる新たな薬剤分子をデザイン可能になります。
当研究室では、現在市販されている医薬品の大半が標的としているGタンパク質共役型受容体(GPCR)やイオンチャネルを対象として、これら膜タンパク質の立体構造解明と新規医薬品のデザインを目指した研究を行っています。
3. 膜タンパク質を標的とする抗体医薬品創出の高効率化に向けた取り組み
 2018年度のノーベル生理学・医学賞でも注目されたがん免疫療法医薬であるオプジーボは膜タンパク質であるPD-1を標的とした抗体医薬です。抗体は、体内に侵入した異物を特異的に認識し、免疫系細胞による処理の際の目印となるタンパク質分子ですが、この標的分子に特異的に結合するという利点を生かし、近年、副作用が少ないバイオ医薬品として大手製薬企業がその開発に力を入れています。しかし、膜タンパク質に対する抗体医薬の創出は困難であることが多く、現状では多大なコストと時間を要する問題があります。
2018年度のノーベル生理学・医学賞でも注目されたがん免疫療法医薬であるオプジーボは膜タンパク質であるPD-1を標的とした抗体医薬です。抗体は、体内に侵入した異物を特異的に認識し、免疫系細胞による処理の際の目印となるタンパク質分子ですが、この標的分子に特異的に結合するという利点を生かし、近年、副作用が少ないバイオ医薬品として大手製薬企業がその開発に力を入れています。しかし、膜タンパク質に対する抗体医薬の創出は困難であることが多く、現状では多大なコストと時間を要する問題があります。
私たちは膜タンパク質の立体構造研究を進める中で、高純度に精製した膜タンパク質を脂質膜環境に再構成したリポソームを抗原として用いることで、従来に比べて高い効率で膜タンパク質に対する抗体が得られることを見出しました(特許第5526448号)。この技術をさらに高度化し、膜タンパク質に対する治療用抗体を迅速に創出可能な技術開発を目指しています。
4. 膜結合型酵素の構造・機能解明および有用物質生産酵素への改変
 酵素は、常温・常圧下で化学反応を進行させる副生成物の少ない有効な触媒として機能します。これまでに、水溶性酵素に関しては多くの研究がなされ、工業利用も行われていますが、膜結合型酵素は単離・精製に特別な注意を要することから、まだまだ立体構造決定や機能の理解が進んでいないのが現状です。
酵素は、常温・常圧下で化学反応を進行させる副生成物の少ない有効な触媒として機能します。これまでに、水溶性酵素に関しては多くの研究がなされ、工業利用も行われていますが、膜結合型酵素は単離・精製に特別な注意を要することから、まだまだ立体構造決定や機能の理解が進んでいないのが現状です。
私たちは、これまでの膜タンパク質の構造生物学研究で蓄積した知識や技術を生かし、このような膜結合型酵素の立体構造決定と機能解明の研究を進めており、特に現在は、原油の主成分であるアルカンを水酸化しアルコールを合成する膜結合型酵素AlkBの立体構造決定と機能改変に向けた研究に注力しています。AlkBは化学的に非常に安定な物質であるアルカンを常温で水酸化することができますが、水酸化可能なアルカンの炭素鎖長は5~12程度に限られています。私たちは、AlkBの立体構造を解明し、部位特異的変異導入により、炭素数4以下のガス状アルカンやベンゼンなどの低分子量芳香族化合物を水酸化可能な人工酵素の創出を目指しています。